Британская компания находится на заключительной стадии клинических испытаний первых в мире фармацевтических препаратов, полученных из конопли, а не из ее синтетического эквивалента, для лечения раковой боли, чтобы вскоре лекарство могло поступить на рынок в США
Испытания, которые проходят на протяжении четверти века, получили одобрение FDA (Управление по контролю за качеством пищевых продуктов и лекарственных препаратов – правительственное агентство США) для испытания отпускаемого по рецепту лекарства на основе основного психоактивного ингредиента конопли.
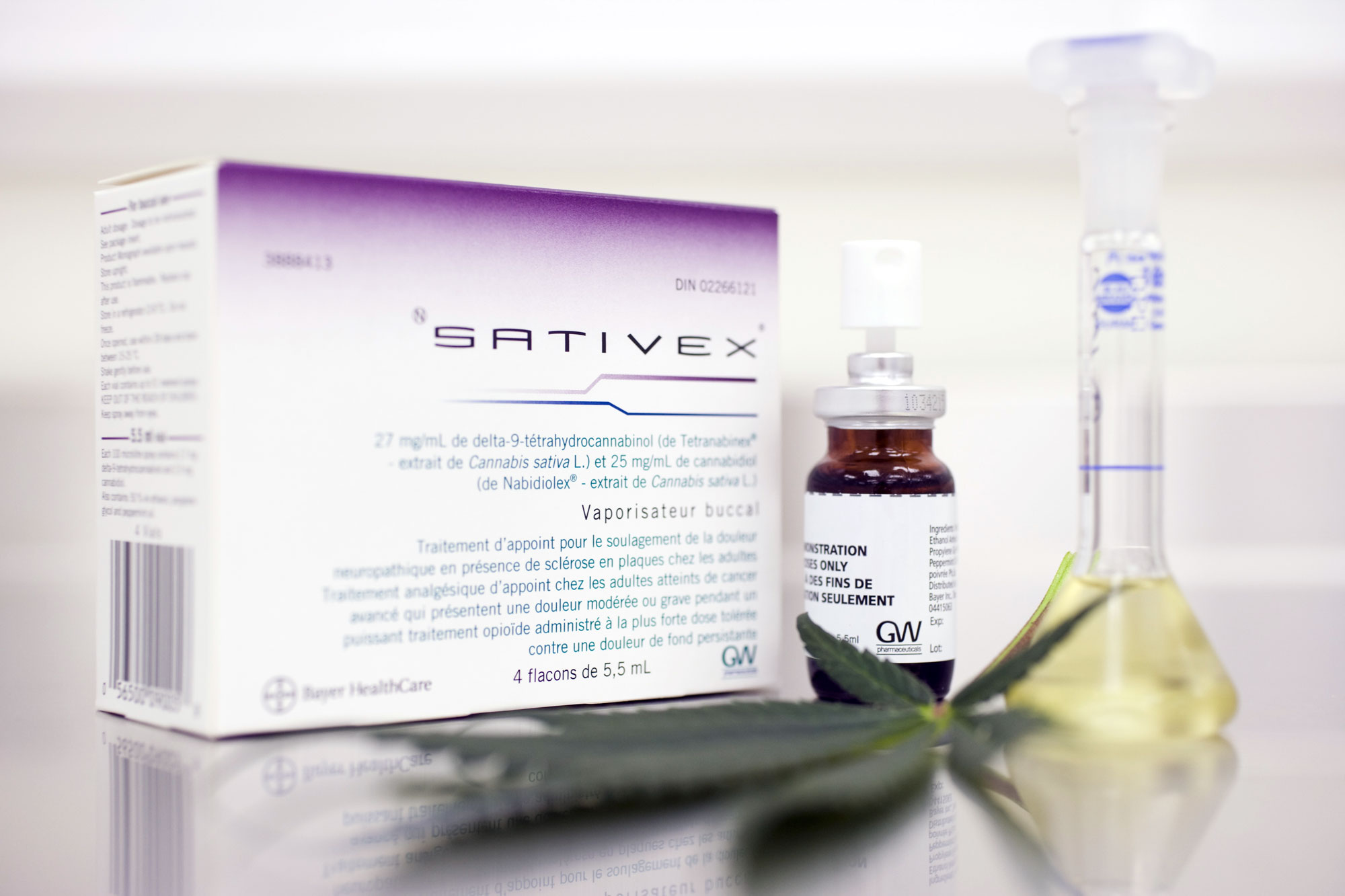
Сативекс — препарат, созданный на основе каннабиноидов, содержащихся в конопле, уже одобрен в Канаде, Новой Зеландии и восьми европейских странах, он предназначен для снятия мышечных спазмов, связанных с рассеянным склерозом.
Выращивание конопли остается в Великобретании незаконным, но около десяти лет назад основателем компании GW Pharmaceuticals, доктором Джеффри Гай было получено разрешение на ее выращивание для разработки рецептурных препаратов. Доктор Гай предложил подойти научно к рассказам о том, что биологические свойства растения помогают больным рассеянным склерозом, а британское правительство одобрило его предложение как потенциальный способ провести четкую грань между рекреационным и медицинским применением конопли.
Национальное общество рассеянного склероза пока еще не одобрило использование конопли пациентами, но спонсирует исследование Университета Калифорнии в Дэвисе, чтобы определить, каким образом применение растения можно сравнить с Маринолом в снятии болезненных мышечных спазмов.
Каннабиноиды, содержащиеся в конопле, в конечном итоге, скорее всего, станут частью врачебного арсенала, если их польза подтвердится клиническими исследованиями.
В дополнение к изучению новых составляющих препарата «Сативекс» компания занимается разработкой других препаратов с использованием конопли.